- История на предметите
- Общи свойства на калай
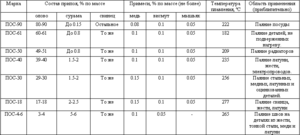
- Сплави на базата на калай
- Използване на елемент и неговите връзки
- Ефекти от тенекиените съединения
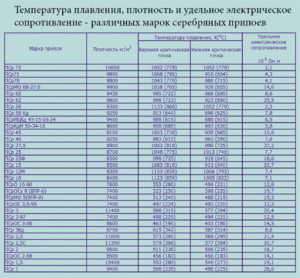 Калайът е мек сребристо-бял метал. Той е толкова ковък и гъвкав, че листовете му с дебелина хиляда милиметър могат да бъдат навити в тръба. Такъв материал се нарича калаена хартия. В периодичната таблица на елементите на Д. И. Менделеев този елемент съответства на число 50, атомно тегло 118, 69 и знак „Sn“ (с латински stannum). 10 от неговите стабилни изотопи са известни. Металът се получава главно от минерала каситерит, който е калаен диоксид.
Калайът е мек сребристо-бял метал. Той е толкова ковък и гъвкав, че листовете му с дебелина хиляда милиметър могат да бъдат навити в тръба. Такъв материал се нарича калаена хартия. В периодичната таблица на елементите на Д. И. Менделеев този елемент съответства на число 50, атомно тегло 118, 69 и знак „Sn“ (с латински stannum). 10 от неговите стабилни изотопи са известни. Металът се получава главно от минерала каситерит, който е калаен диоксид.
За запояване се използва предимно метал в сплав с олово. В допълнение, той се използва като антикорозионно покритие за съдове от хранителна стомана, тъй като е нетоксичен. Композитите с калай се използват като фунгициди, бои, паста за зъби (SnF2) и керамика.
История на предметите
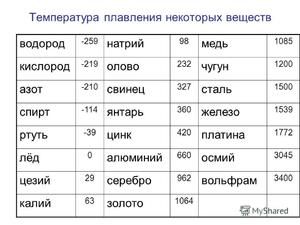 Този елемент е открит през 1854 г. от Халюс Пелегрин. Използването му обаче започва много преди тази дата в Близкия изток и на Балканите около 2000 г. пр.н.е. В тази епоха е открит бронз (сплав от калай и мед), който дава името на бронзовата епоха. Те произвеждаха бронзови оръжия и инструменти, които бяха по-ефективни от камък и кост.
Този елемент е открит през 1854 г. от Халюс Пелегрин. Използването му обаче започва много преди тази дата в Близкия изток и на Балканите около 2000 г. пр.н.е. В тази епоха е открит бронз (сплав от калай и мед), който дава името на бронзовата епоха. Те произвеждаха бронзови оръжия и инструменти, които бяха по-ефективни от камък и кост.
В древни времена производството на бронз води до развитие на търговията между различни страни. В Стария Завет има и препратки към този метал. И така, в Месопотамия те правели бронзови оръжия, а в Древен Рим покривали с калай вътрешната повърхност на медни съдове, за да увеличат устойчивостта си на корозия.
Общи свойства на калай
Всички свойства на този метал могат да бъдат разделени на две големи групи : физични и химични.
Физически характеристики
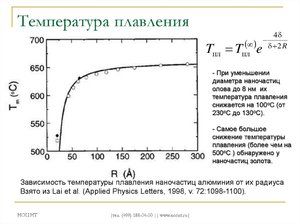 Това е сребрист ковък метал, който лесно се окислява при температура на околната среда, докато цветът на калай се променя до тъмносив. Ако огънете плоча от този метал, можете да чуете характерен звук, така наречения „калайдисване“, който се получава поради триене между съставните му кристали. Една от изразените му характеристики е рязко влошаване на механичните свойства при определени условия, наречени „калаена чума“: под -18 ° C металът се разрушава и започва да изглежда като сив прах.
Това е сребрист ковък метал, който лесно се окислява при температура на околната среда, докато цветът на калай се променя до тъмносив. Ако огънете плоча от този метал, можете да чуете характерен звук, така наречения „калайдисване“, който се получава поради триене между съставните му кристали. Една от изразените му характеристики е рязко влошаване на механичните свойства при определени условия, наречени „калаена чума“: под -18 ° C металът се разрушава и започва да изглежда като сив прах.
Чистият калай има две алотропни модификации: сива и бяла. Сивата модификация има кубична кристална структура, е полупроводник, много крехка, има ниска плътност и е стабилна при температури под 13, 2 ° C. Бялата алотропна модификация има тетрагонална кристална структура, провежда добре електрически ток и е стабилна при температури над 13, 2 ° C.
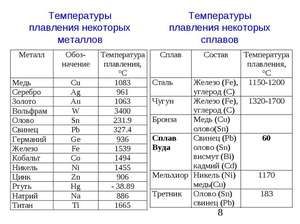
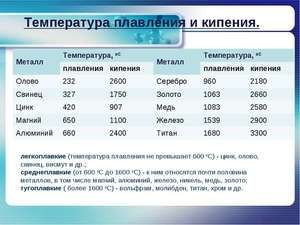
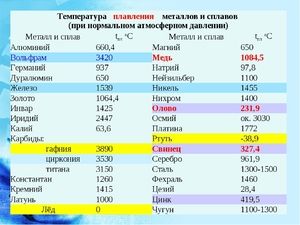
Металът се стопява при сравнително ниска температура от 232 ° C (за сравнение: желязото се топи при 1535 ° C). Необходимо е да се разбере, отговаряйки на въпроса, при каква температура се топи калай, каква точно е топенето на нейната бяла алотропна модификация. Въпреки ниската точка на топене, кипенето на метала става при сравнително висока температура от 2602 ° С (желязото кипи при 2750 ° С).
Химични свойства
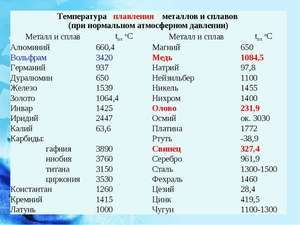 Най-важният минерал е каситерит, SnO2. Понастоящем неизвестни рудни находища с висок процент на този минерал. Повечето от каситеритите в света се добиват от нискокачествени алувиални наноси. Именно от този минерал се произвежда калай в промишлен мащаб. За това каситеритът се стрива до получаването на неговия концентрат и след това се топи заедно с кокс, кварц и вар в доменна пещ. След това отливки под формата на блокове преминават окончателното почистване от примеси от бисмут, мед и желязо.
Най-важният минерал е каситерит, SnO2. Понастоящем неизвестни рудни находища с висок процент на този минерал. Повечето от каситеритите в света се добиват от нискокачествени алувиални наноси. Именно от този минерал се произвежда калай в промишлен мащаб. За това каситеритът се стрива до получаването на неговия концентрат и след това се топи заедно с кокс, кварц и вар в доменна пещ. След това отливки под формата на блокове преминават окончателното почистване от примеси от бисмут, мед и желязо.
Химическият елемент калай реагира добре както със силни киселини, така и със силни основи, но е относително инертен в неутрални разтвори. Корозира в присъствието на окисляваща среда, при липса на кислород металът на практика не корозира. По време на окисляването върху металната повърхност се образува плътен оксиден филм, който предпазва останалата част от по-нататъшно окисляване.
 Ако при разтваряне на соли във вода се образува кисела среда, тогава в присъствието на окислители или въздух, калайът реагира. Такива соли включват хлориди, например алуминий и желязо. Повечето неводни течности, като масла и алкохоли, практически не реагират с калай. Самият калай и неговите прости неорганични соли не са токсични, но някои органични композити са токсични.
Ако при разтваряне на соли във вода се образува кисела среда, тогава в присъствието на окислители или въздух, калайът реагира. Такива соли включват хлориди, например алуминий и желязо. Повечето неводни течности, като масла и алкохоли, практически не реагират с калай. Самият калай и неговите прости неорганични соли не са токсични, но някои органични композити са токсични.
Калаеният (II) оксид, SnO е черно-син кристал, който се разтваря в киселини и основи. Използва се за производството на соли при галванопластика и при производството на стъкло. Калаеният (IV) оксид, SnO2 е бял прах, неразтворим в киселини. Използва се като незаменим компонент за оцветяване в розова, жълта и кафява керамика, както и в диелектрици и огнеупорни сплави. Той е важен агент при полирането на мрамор и други декоративни камъни.
Калаеният (II) хлорид, SnCl2 е основната съставка в калаената киселина за запояване. Калаеният (IV) хлорид, SnCl4 се използва като химическа съставка за придаване на тегло на копринената тъкан, както и за стабилизиране на определени парфюмни продукти и стабилизиране на цвета на сапуна, а SnF2, който е бял и разтворим във вода, се използва като добавка към пастите за зъби.
Органичните химични съединения на базата на този елемент са онези съединения, в които присъства най-малко една калаено-водородна връзка, Sn-H и в които металът има окислително състояние от +4. Органичните съединения, намерили приложение в индустрията, имат следните химични формули:
- R4Sn;
- R3SnX;
- R2SnX2;
- RSnX3.
Тук R е органична група, например, метил, етил, бутил и други, а X е неорганичен елемент, например хлор, кислород, флора и други.
Сплави на базата на калай
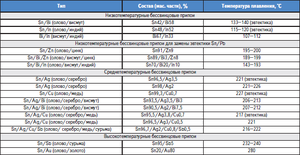 Сплавите на базата на калай също са известни като бели метали, обикновено съдържащи мед, антимон и олово. Сплавите имат различни механични свойства в зависимост от техния състав.
Сплавите на базата на калай също са известни като бели метали, обикновено съдържащи мед, антимон и олово. Сплавите имат различни механични свойства в зависимост от техния състав.
Калаените и оловни сплави са намерили търговската си употреба за широк спектър от съединения. Така 61, 9% калай и 38, 1% олово съответстват на евтектичния състав, чиято степен на втвърдяване е 183 ° С. Сплавите с различно съотношение на тези метали се стопяват и кристализират в широк температурен диапазон, когато има равновесие между твърдата и течната фаза. При такава кристализация твърдите сегрегации започват да се утаяват в стопилката, което води до образуването на различни структури. Евтектичната сплав, тъй като има най-ниската точка на топене, се използва като защита срещу прегряване на електронни компоненти.
Има и сплави, в които освен тези метали присъства и малко количество антимон (до 2, 5%). Основният проблем на сплавите на основата на калай и олово е отрицателното им въздействие върху околната среда, поради което наскоро са разработени техни заместители, в които оловото не се използва, например сплави със сребро и мед.
Сплавите от калай с олово и антимон се използват за декоративни бижута, а някои сплави от калай, мед и антимон се използват като смазка за намаляване на триенето в лагерите, поради антифрикционните им свойства. В допълнение към горните сплави, калайът се използва в бронзови сплави и в сплави с титан и цирконий.
Използване на елемент и неговите връзки
Всички области на човешкото производство, в които този елемент се използва пряко или косвено, са изброени по-долу:
 Защита срещу корозия и механично натоварване на стомани и други метали, например при производството на консерви;
Защита срещу корозия и механично натоварване на стомани и други метали, например при производството на консерви;- Намаляване на чупливостта на стъклото, както и при производството на огледала;
- В гонени шарки на различни ястия;
- Използвайте в фунгициди, бои, пасти за зъби и различни пигменти.
- При получаване на различни сплави, например, бронзи.
- За нискотемпературно запояване или меко запояване;
- Съставен с олово в производството на метални листове за музикални инструменти;
- Чрез производство на етикети на различни продукти;
- В сплави, които предпазват от прегряване на електрически апарати и електронни микросхеми;
- В керамичната промишленост за производство на емайли като матиращ агент.
- В капсули за закупуване на бутилки за вино. Производството на такива капсули се разшири след забраната за използване на олово в хранителната промишленост.
Ефекти от тенекиените съединения
Активността на съединенията с този елемент, по един или друг начин, засяга както човешкото тяло, така и околната среда.
За здравето на хората
 Както вече споменахме, най-опасни за човешкото здраве са органичните химични съединения на калай. Тези вещества се използват широко в промишлеността, например при производството на бои, пластмаси и пестициди за селското стопанство. Освен това производството на органични съединения с този метал непрекъснато нараства, въпреки факта, че последствията от отравянето от тях са известни .
Както вече споменахме, най-опасни за човешкото здраве са органичните химични съединения на калай. Тези вещества се използват широко в промишлеността, например при производството на бои, пластмаси и пестициди за селското стопанство. Освен това производството на органични съединения с този метал непрекъснато нараства, въпреки факта, че последствията от отравянето от тях са известни .
Ефектите на тези вещества върху хората са разнообразни, всичко зависи от вида на съединението и от индивидуалните характеристики на организма. Опасността от съединението корелира с дължината на връзката между метала и водорода, колкото по-дълга е тази връзка, толкова по-малко опасна е връзката. В тази връзка съединението на калай с три етилови групи, водородните връзки на които са сравнително къси, се счита за най-опасното органично вещество.
Тези вещества могат да попаднат в човешкото тяло чрез храна, чрез въздушни капчици или просто да ги докоснат. Известни са следните ефекти от въздействието на органичните калаени съединения върху човешкото тяло:
- Когато сте в стая, съдържаща пари от този метал, силно дразнене на горните дихателни пътища, кожата и очите;
- Главоболие, стомашни болки и липса на апетит;
- Гадене и повръщане;
- Проблеми с уринирането;
- Силно изпотяване и задух.
Изброените ефекти могат да доведат до по-сериозни последици:
- депресия;
- Чернодробни проблеми;
- Нарушена имунна система
- Увреждане на хромозомите на клетките и липса на червени тела в кръвта;
- Увреждане на мозъка (нарушения на съня, главоболие, неуспехи в паметта, раздразнено състояние).
Към околната среда
 Както калаените атоми, така и самият метал в чисто състояние не са токсични за нито един организъм на земята, от своя страна почти всички съединения с този елемент от органичен характер са вредни. Тези съединения могат да бъдат в околната среда за дълъг период от време. Те са доста стабилни и практически не се разлагат под въздействието на микроорганизми, поради силните си водородни връзки. Колкото и малка да е концентрацията на съединенията на този метал в почвата и водата, с оглед на гореизложеното, те постоянно нарастват.
Както калаените атоми, така и самият метал в чисто състояние не са токсични за нито един организъм на земята, от своя страна почти всички съединения с този елемент от органичен характер са вредни. Тези съединения могат да бъдат в околната среда за дълъг период от време. Те са доста стабилни и практически не се разлагат под въздействието на микроорганизми, поради силните си водородни връзки. Колкото и малка да е концентрацията на съединенията на този метал в почвата и водата, с оглед на гореизложеното, те постоянно нарастват.
Известно е, че органичните калаени съединения причиняват голяма вреда на водните екосистеми, тъй като са токсични за гъбички, водорасли и фитопланктон. Фитопланктонът е важна част от водната екосистема, тъй като произвежда кислород за всички останали живи организми от тази система, а също така е важна част в хранителната верига. Токсичността на калаените съединения е различна за различните живи същества, например трибутил калаят е токсичен за рибата и гъбите, докато трифеноловият калай е най-токсичното съединение за фитопланктона.
Известно е също така, че органичните съединения на този елемент имат отрицателен ефект върху растежа и репродуктивната функция на животните, нарушават функционирането на ензимите. Такива съединения се натрупват главно в горните слоеве на почвата и водата.